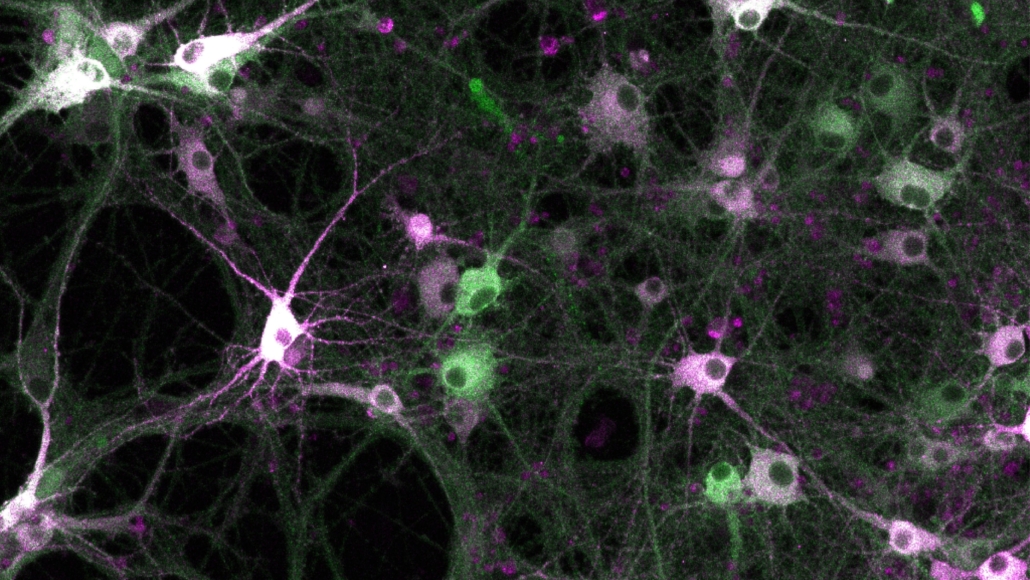
Neues Verfahren zeichnet Kinase-Aktivität in-vivo auf
Wissenschaftler des Max-Planck-Instituts für medizinische Forschung in Heidelberg haben ein molekulares Werkzeug entwickelt, mit dem sich die Aktivität von Proteinkinasen in lebenden Zellen präzise und dauerhaft aufzeichnen lässt.
Das von De-en Sun (Universität Peking) und Kai Johnsson (MPI für medizinische Forschung) Kinprola genannte System basiert auf dem gespaltenen HaloTag-Protein, einem biotechnologisch modifizierten Enzym, das sich in Anwesenheit eines fluoreszierenden Substrats wie Tetramethylrhodamin (TMR) selbstständig markiert, sobald es durch eine spezifische Kinaseaktivität modifiziert wird.
Im Zentrum von Kinprola steht ein molekularer Schalter, der durch die Phosphorylierung eines Peptidmotivs ausgelöst wird. Ist eine Zielkinase wie Protein Kinase A (PKA) aktiv und gleichzeitig das fluoreszierende Substrat vorhanden, wird Kinprola irreversibel markiert. Die Stärke der Fluoreszenz korreliert mit dem Ausmaß der Kinaseaktivität, während das Substrat-Zeitfenster die Dauer der Aufzeichnung bestimmt. Die Methode ermöglicht es, flüchtige zelluläre Signalprozesse auch in Geweben sichtbar zu machen, die für klassische Mikroskopieverfahren unzugänglich sind. Dabei kann die Analyse zeitlich von der Aufzeichnung entkoppelt werden. Zellen mit registrierter Kinaseaktivität lassen sich gezielt mittels Durchflusszytometrie isolieren und anschließend mit Transkriptomanalysen oder genetischen Screens weiter charakterisieren. In Tierversuchen ließ sich etwa im Mausgehirn nach pharmakologischer Stimulation eine PKA-Aktivierung detektieren.
„Wir wollten einen Weg finden, Kinaseaktivitäten skalierbar und hochauflösend aufzuzeichnen, ohne durch die bisherigen Begrenzungen der optischen Bildgebung eingeschränkt zu sein. Unter dem Mikroskop sind Beobachtungen in der Regel auf die Echtzeit-Bildgebung einer relativ kleinen Anzahl von Zellen beschränkt und lassen sich nicht ohne Weiteres auf tiefliegende Gewebe übertragen“, so De-en Sun. Mit ihrem molekularen Rekorder Kinprola haben die Wissenschaftler einen Weg gefunden, die Grenzen der optischen Echtzeitaufzeichnung zu überwinden. Für die Wirkstoffentwicklung eröffnet Kinprola neue Perspektiven: Es erlaubt die systematische Analyse, wie Medikamentenkandidaten in komplexen zellulären Kontexten auf bestimmte Signalwege wirken – und das nicht nur in Zelllinien, sondern auch in vivo. In Verbindung mit CRISPR-Funktionsscreens lassen sich zudem neue molekulare Zielstrukturen oder Resistenzmechanismen identifizieren. Subtile, ortsabhängige Effekte von Wirkstoffen, die bisher übersehen wurden, können so gezielt untersucht und therapeutisch genutzt werden.
Die Technik wurde gemeinsam mit dem Deutschen Krebsforschungszentrum, der Universität Heidelberg und der Peking-Universität entwickelt und stellt unter dem Gesichtspunkt der „spatial biology“, also der zeitlich-räumlichen Auflösung von Reaktionen, ein neues Instrument für biomedizinische Grundlagenforschung und translational orientierte Arzneimittelentwicklung dar.

 freshidea - stock.adobe.com
freshidea - stock.adobe.com Pharvaris Holdings B.V.
Pharvaris Holdings B.V. Coriolis Pharma Research GmbH
Coriolis Pharma Research GmbH